Показана возможность создания натрий-ионных аккумуляторных батарей, работающих при комнатной температуре
16 февраля 2012 в 12:00
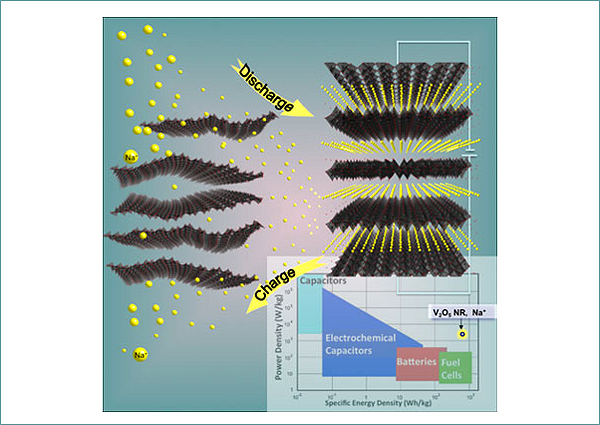
Учёные из Аргоннской национальной лаборатории и Чикагского университета (оба — США) объявили о разработке высокоэффективных 3V-катодов для аккумуляторных натрий-ионных батарей. Эти двухслойные V2O5-системы, обладающие теоретической ёмкостью в 250 мА∙ч/г, мощностью в 1 200 Вт/кг и плотностью энергии ~760 Вт∙ч/кг, выдерживающие большое число проходящих с высокой скоростью циклов перезарядки, могут применяться при комнатной температуре.
Перезаряжаемые батарейные системы с транспортными ионами, отличными от ионов лития, могли бы стать альтернативой литий-ионным батареям, что существенно расширило бы существующий рынок аккумуляторов, которые, как мы знаем, в основном базируются на литий-ионной технологии. Идея батарей на ионах натрия всегда была особенно привлекательной. Начнём с того, что натрий дешевле почти в 30 раз, хотя оба элемента получают из расплавов солей при примерно одинаковой температуре 600–700 ˚C. Правда, хлорид лития смешивают с дорогим хлоридом калия для понижения температуры плавления, а хлорид натрия — с гораздо более дешёвым хлоридом кальция. Но не в этом основная причина дороговизны (хотя и в этом тоже), а в исходном сырье.
Электростатическое притяжение электрохимически изменённых слоёв оксида ванадия создаёт сильную движущую силу для ионов натрия Na+.
Хлорид натрия, поваренная соль, один из основных минералов натрия — бери и используй. Литий же, решивший усложнить нам жизнь, вырабатывается в основном в виде литий-алюминиевых силикатов (та же глина, только не натриевая, а литиевая), существующих в двух формах: альфа (твёрдая) и бета (более мягкая и более реакционно способная). В природе, конечно же, распространена альфа-форма, её нагревают до ~1 000 ˚C, переводя в бета-форму (счётчик расхода энергии только что раскрутился до покраснения), а затем действуют горячей серной кислотой для получения сульфата лития, который экстрагируют водой; после этого раствор обрабатывают содой для осаждения нерастворимого карбоната лития. Последний штрих — воздействие на осадок раствором соляной кислоты — приводит к получению хлорида лития в водном растворе и парникового газа в заводской трубе. Вот за всю эту химию и приходится в конечном итоге расплачиваться потребителю.
На этом фоне натрий смотрится Золушкой на царском балу. То есть всё при нём, но чего-то не хватает... А не хватает обычно малости. Либо рабочие температуры натриевых батарей начинаются с 65 ˚C, что не очень высоко, но уже никому не интересно (это для натрий-серных, не ионных), либо, как в случае с натрий-ионными батареями, низкая ёмкость, короткая жизнь и невозможность поддерживать начальный уровень заряда уже после нескольких циклов перезарядки.
В данном же исследовании, и это стоит подчеркнуть особо, речь идёт о создании натрий-ионной батареи, работающей при комнатной температуре и обладающей выдающимися электрическими характеристиками, даже по сравнению с литиевыми аналогами.
Кроме того, соли натрия, тот же хлорид, не токсичны, в отличие от солей лития (см. LiCl). Натрий равномерно распределён по планете (а вот залежи литиевых минералов имеют центры концентрации, например, в Афганистане существует море — всё сплошь из соли. Считается, что соль этого месторождения чрезвычайно богата именно хлоридом лития. Не на неё ли позарились доблестные «морские котики»?). Всё это делает натрий идеальным транспортным ионом для аккумуляторных батарей.
В рассматриваемой работе учёные попытались добиться интеркаляции натрия, используя наноразмерные материалы, имеющие структуру двумерных слоев с межслоевым расстоянием, способным изменяться в очень широких пределах. В качестве слоистого материала был выбран оксид ванадия, чьи наноструктуры получаются методом электрохимического осаждения. Дальнейшее еx-situ- и in-situ-изучение полученной системы на синхротроне показало, что интеркаляция натрия между слоёв оксида ванадия вызывает появление как ближнего, так и дальнего порядка. В то время как выход ионов натрия приводит к потере дальнего порядка при сохранении ближнего. Таким образом, высоко упорядоченный наноматериал с максимальным количеством интеркалированного натрия способен достигать теоретической обратимой ёмкости в 250 мА∙ч/г для Na2V2O5-стехиометрии.
Результат, достигнутый в исследовании и представленный в журнале ACS Nano, наглядно демонстрирует осуществимость разработки натрий-ионных аккумуляторных батарей, работающих при комнатной температуре и обладающих великолепными электрическими показателями.
Никто пока не комментировал эту страницу.